Recorde de bioinsumos na agricultura em 2025: o que os 912 registros do MAPA mostram para o mercado

Sumário
Bionsumos na agricultura em 2025: Recorde de 912 registros concedidos pelo MAPA. Entenda os impactos regulatórios, dados do Ibama e tendências para o setor.
O recorde de bioinsumos 2025 marca um dos movimentos mais relevantes do setor regulatório agrícola nos últimos anos. Segundo o Ministério da Agricultura e Pecuária, o Brasil encerrou 2025 com 912 registros concedidos, incluindo 323 produtos técnicos e 162 bioinsumos, o maior número já registrado nessa categoria. Esse avanço não representa apenas aumento de volume. Ele sinaliza uma mudança importante no perfil do mercado, na dinâmica concorrencial e na estratégia regulatória das empresas.
O tema interessa diretamente a fabricantes, formuladores, distribuidores, consultorias regulatórias e áreas de inteligência de mercado. Afinal, um volume maior de registros tende a aumentar a competição, acelerar revisões de portfólio e exigir mais capacidade de gestão técnica e documental. Em paralelo, os dados de produtos formulados deferidos em 2025 ajudam a entender melhor a composição desse movimento, revelando quais formatos, classes ambientais e ingredientes ativos tiveram maior presença ao longo do ano.
Em termos práticos, o recorde de bioinsumos na agricultura em 2025 reforça que a agenda regulatória brasileira está se tornando mais estratégica. Não basta acompanhar publicações oficiais ou olhar apenas para o número de registros concedidos. É preciso interpretar o que esses dados significam para o pós-registro, para a preparação documental do produto e para a capacidade das empresas de colocar no mercado itens acompanhados de rótulos, bulas e FDS consistentes e tecnicamente bem estruturados.
O que mudou com o recorde de bioinsumos na agricultura em 2025
O principal destaque do ano foi o crescimento dos bioinsumos na agricultura. O MAPA informou que, em 2025, foram liberados 162 registros de bioinsumos, incluindo produtos formulados biológicos, microbiológicos, bioquímicos, extratos vegetais, reguladores de crescimento e semioquímicos, inclusive para uso na agricultura orgânica. O dado é relevante porque mostra que o segmento deixou de ser periférico e passou a ocupar um espaço mais robusto na pauta regulatória e comercial.
Esse crescimento também acompanha mudanças mais amplas no setor. O mercado busca soluções com maior eficiência, novas combinações tecnológicas, alternativas para manejo integrado e respostas às demandas por sustentabilidade. Nesse contexto, o recorde de bioinsumos 2025 deve ser lido como sinal de amadurecimento regulatório e de expansão competitiva.
Outro aspecto importante é que esse avanço ocorreu em um ambiente de reorganização normativa. A Lei nº 14.785/2023 consolidou um novo marco legal para os agrotóxicos, produtos de controle ambiental, produtos técnicos e afins, abrangendo etapas como pesquisa, produção, embalagem, rotulagem, transporte, armazenamento, comercialização, importação, exportação, registro, inspeção e fiscalização. Esse contexto ajuda a explicar por que 2025 teve forte movimentação administrativa e regulatória.
Para os fabricantes, porém, o aumento dos registros não representa apenas mais concorrência ou mais opções tecnológicas. Ele também amplia a necessidade de organizar a etapa posterior ao deferimento, especialmente na elaboração dos documentos que acompanham o produto. É nesse ponto que rótulos, bulas e FDS ganham peso operacional, porque ajudam a transformar o registro aprovado em produto efetivamente preparado para circulação, comunicação técnica e uso no mercado.
Como ler os 912 registros concedidos pelo MAPA
O número de 912 registros concedidos chama atenção, mas precisa ser interpretado com critério. O próprio MAPA esclareceu que registro não equivale automaticamente a uso ou comercialização em larga escala. O desempenho de mercado depende de fatores como área plantada, condições climáticas, pressão de pragas, estratégia comercial e aceitação técnica pelo produtor. Além disso, entre o deferimento regulatório e a efetiva entrada do produto no mercado existe uma etapa prática muitas vezes subestimada: a preparação da documentação que acompanha o produto, como rótulos, bulas e FDS.
Ainda assim, o total de registros concedidos em 2025 mostra um ambiente regulatório muito ativo. Para a indústria, isso significa mais competição em diversas frentes. Para quem trabalha com compliance, o dado indica necessidade de reforçar governança, monitoramento de pós-registro, inteligência sobre posicionamento de portfólio e organização documental para que o produto chegue ao mercado com informações claras, seguras e coerentes.
Quantos bioinsumos na agricultura foram liberados
Dentro dos 912 registros, o grupo mais simbólico foi o dos 162 bioinsumos. Esse número mostra a força crescente de soluções biológicas e correlatas no mercado brasileiro. Mais do que um dado estatístico, ele aponta para uma mudança na lógica de inovação do setor.
Empresas que já atuam com essa categoria ganham um sinal positivo de mercado, mas também enfrentam aumento da concorrência. Já aquelas que ainda não estruturaram estratégia para bioinsumos na agricultura passam a ter um alerta claro: o segmento tende a ganhar ainda mais espaço na agenda regulatória e comercial.
Esse avanço também tem efeito direto na rotina documental das empresas. Quanto maior o número de bioinsumos e produtos formulados entrando no mercado, maior a necessidade de preparar materiais que sustentem o uso correto e a comunicação técnica do produto. Em muitos casos, a qualidade de rótulos, bulas e FDS passa a ser decisiva para evitar retrabalho, padronizar informações e dar suporte ao lançamento comercial.
O peso dos produtos técnicos e dos ingredientes ativos novos
O MAPA também informou que 2025 terminou com 323 produtos técnicos registrados. Essa categoria é especialmente relevante para uso industrial e para a cadeia de formulação. Além disso, o ano registrou 6 produtos técnicos com ingredientes ativos novos e 19 produtos formulados à base de ingrediente ativo novo.
Esse dado é importante porque mostra que o avanço de 2025 não se resumiu a equivalentes ou à repetição de soluções já consolidadas. Houve também entrada de novas tecnologias e novos modos de ação, o que tende a ampliar possibilidades de manejo, inovação e competição técnica.
Do ponto de vista regulatório, isso aumenta a necessidade de leitura estratégica. Um mercado com mais produtos técnicos e mais ingredientes ativos novos exige que as empresas revisem seus movimentos de registro, parceria, distribuição e diferenciação.
Na prática, produtos novos ou com posicionamentos mais específicos também podem demandar maior cuidado na forma como serão apresentados ao mercado. Isso inclui a elaboração de rótulos, bulas e FDS compatíveis com as características do produto, com linguagem técnica adequada e informações organizadas para apoiar distribuição, orientação de uso e comunicação de segurança.
O que os dados de produtos formulados deferidos em 2025 revelam
Além do balanço anual do MAPA, os dados de produtos formulados deferidos pelo Ibama em 2025 ajudam a enxergar melhor a composição do mercado. Nesse recorte, foram observados 470 produtos formulados deferidos ao longo do ano. Esse volume, por si só, já mostra que houve uma atividade expressiva na aprovação de produtos formulados e reforça a necessidade de estruturação do pós-registro, inclusive no preparo de rótulos, bulas e FDS para produtos que avançam para a etapa comercial.
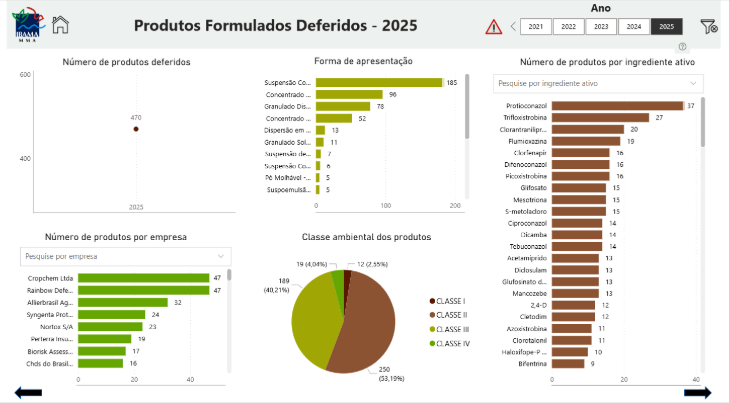
Produtos formulados deferidos em 2025, destacando volume total, formas de apresentação, classes ambientais e ingredientes ativos mais frequentes (fonte Ibama)
Mais do que isso, os dados permitem entender como esse volume se distribui entre formas de apresentação, empresas, classes ambientais e ingredientes ativos. Essa leitura é valiosa porque transforma um número amplo em sinais concretos de tendência regulatória e competitiva.
Formas de apresentação mais frequentes
Entre as formas de apresentação com maior presença, a suspensão concentrada lidera com 185 produtos, seguida por uma categoria concentrada com 96 registros e por granulado dispersível, com 78. Outra forma concentrada aparece com 52 produtos. As demais categorias exibidas têm participação menor.
Esse padrão sugere concentração em formatos já amplamente utilizados no mercado. Para empresas do setor, isso significa que a competição não está só no ingrediente ativo, mas também na formulação, na estabilidade, na logística, na aplicabilidade e no posicionamento comercial do produto.
Em outras palavras, a análise dos formulados deferidos mostra que o mercado continua valorizando formatos tecnicamente consolidados. Isso ajuda a explicar por que a gestão de portfólio segue sendo central: o diferencial competitivo nem sempre está em lançar algo totalmente novo, mas em lançar com agilidade, robustez documental e boa estratégia de mercado.
Essa robustez documental não se limita ao processo regulatório em sentido estrito. Ela também aparece nos documentos que acompanham o produto após sua aprovação. Empresas com maior volume de produtos ou com portfólio diversificado tendem a enfrentar mais desafios de padronização, revisão e atualização de rótulos, bulas e FDS, especialmente quando precisam manter consistência entre diferentes formulações e linhas comerciais.
Classe ambiental e ingredientes ativos com maior presença
Na divisão por classe ambiental, os dados mostram predominância de Classe II, com 250 produtos (53,19%), seguida de Classe III, com 189 produtos (40,21%). As Classes IV e I aparecem com participação menor, com 19 produtos (4,04%) e 12 produtos (2,55%), respectivamente.
Essa distribuição sugere concentração em faixas intermediárias de classificação ambiental. Para as empresas, isso reforça a importância de tratar avaliação ambiental como parte estratégica do desenvolvimento, do dossiê e do posicionamento regulatório.
No recorte por ingrediente ativo, os destaques são protioconazol, com 37 produtos, e trifloxistrobina, com 27. Também aparecem com presença relevante ingredientes como clorantraniliprole, flumioxazina, clorfenapir, difenoconazol, picoxistrobina, glifosato, mesotriona e S-metolacloro, entre outros.
Essa concentração revela um mercado ainda fortemente apoiado em moléculas já conhecidas, com dinâmica intensa de equivalência, formulação e reposicionamento competitivo. Isso dialoga com a própria leitura do MAPA de que grande parte dos registros concedidos corresponde a produtos equivalentes.
Para os fabricantes, isso significa que o desafio competitivo não está apenas em registrar ou posicionar o produto, mas também em comunicar corretamente suas características ao mercado. Em cenários com produtos equivalentes, diferentes formulações ou linhas próximas entre si, documentos como rótulo, bula e FDS ganham importância adicional para organizar informações, evitar inconsistências e sustentar uma comunicação técnica mais confiável.
Impactos práticos para fabricantes, registrantes e distribuidores após o recorde de registros de bioinsumos no setor agrícola
O recorde de bioinsumos na agricultura em 2025 gera efeitos práticos imediatos. O primeiro deles está na revisão de portfólio. Empresas precisam entender onde estão suas oportunidades reais: bioinsumos, equivalentes, produtos técnicos, ingredientes ativos novos ou combinações entre essas frentes. Mas esse movimento também exige olhar com mais atenção para a etapa posterior ao deferimento, quando o produto precisa ser preparado documentalmente para chegar ao mercado e isso inclui a necessidade de preparar o produto para o mercado com rótulo, bula e FDS tecnicamente consistentes e alinhados às exigências aplicáveis.
O segundo impacto está na concorrência. Quanto maior o número de registros concedidos, maior a tendência de saturação em certas categorias e maior a necessidade de diferenciação. Isso exige atuação mais integrada entre regulatório, marketing, inteligência de mercado e área comercial.
Portfólio, concorrência e tempo regulatório
Para quem atua no setor, um registro concedido não pode ser visto como ponto final. Ele é apenas uma etapa. O valor real aparece quando o deferimento é convertido em produto lançado, cadeia abastecida, documentação em ordem e estratégia de mercado consistente. Nesse contexto, a elaboração de rótulos, bulas e FDS deixa de ser apenas uma formalidade documental e passa a ser parte prática da preparação do produto para comercialização e uso.
Nesse ponto, o recorde de bioinsumos na agricultura em 2025 traz uma lição clara: empresas com capacidade de transformar aprovação regulatória em execução comercial tendem a capturar mais valor. Já organizações com baixa integração entre áreas podem ter produto aprovado, mas demorar para gerar resultado concreto.
O aumento do número de deferimentos também pressiona o tempo de resposta das empresas. Quanto mais competitivo o mercado, menos espaço existe para lentidão em revisão documental, ajustes de rótulo, atualização cadastral, planejamento de estoque e estruturação comercial.
Governança documental e estratégia de pós-registro
Outro efeito importante está na governança documental. O MAPA informou que 2025 teve mudanças de fluxo, incluindo centralização e uniformização de protocolo, distribuição e tramitação de pedidos de registro e pós-registro, com uso do SEI/Mapa para novos pleitos a partir de setembro.
Esse tipo de mudança exige mais disciplina de processo. Empresas precisam controlar melhor documentos, versões, comprovantes, exigências e histórico interno de atualização. Em um cenário com mais registros e maior complexidade, o pós-registro ganha relevância estratégica. Isso inclui organizar com cuidado documentos como rótulos, bulas e FDS, que precisam acompanhar a evolução do portfólio com clareza e consistência.
Também vale lembrar que o sistema de avaliação continua dependente da análise tripartite entre MAPA, Anvisa e Ibama. Isso significa que o sucesso regulatório depende de coordenação técnica, leitura integrada de requisitos e preparação mais robusta dos dossiês.
Na prática, muitas empresas concentram esforços na obtenção do registro, mas descobrem depois que o lançamento depende de uma segunda frente igualmente crítica: a entrega correta dos documentos que acompanham o produto. Um rótulo mal estruturado, uma bula incompleta ou uma FDS desatualizada podem gerar retrabalho, atrasar a entrada no mercado e aumentar a exposição regulatória e operacional da empresa.
Tendências regulatórias para 2026
Os sinais para 2026 apontam continuidade da modernização regulatória. O MAPA associou as medidas recentes à implementação da Lei nº 14.785/2023 e à evolução dos sistemas eletrônicos, incluindo a preparação do Sistema Unificado de Informação, Petição e Avaliação Eletrônica (SISPA).
Na prática, isso indica que o ambiente regulatório deve se tornar mais digital, mais rastreável e potencialmente mais exigente em qualidade documental. Não basta protocolar. Será cada vez mais importante protocolar com coerência, consistência técnica e visão estratégica.
O recorde de bioinsumos na agricultura em 2025 tende, portanto, a funcionar como base para uma nova fase. Empresas que usarem 2026 para qualificar processos internos podem ganhar vantagem competitiva. Quem mantiver atuação apenas reativa tende a enfrentar mais retrabalho e menor previsibilidade.
Checklist regulatório para empresas
1. Reclassifique o portfólio
Separe produtos equivalentes, bioinsumos, técnicos e formulações com maior potencial de mercado.
2. Revise o pipeline regulatório
Avalie registros concedidos, processos em andamento, pós-registro e necessidade de atualização documental.
3. Cruze regulação com mercado
Observe quais ingredientes ativos e formas de apresentação estão mais presentes para entender densidade concorrencial.
Observe quais ingredientes ativos e formas de apresentação estão mais presentes para entender densidade concorrencial.
4. Reforce a integração entre áreas
Regulatório, comercial, supply e marketing precisam operar com a mesma leitura estratégica.
5. Fortaleça a governança documental
Mudanças de fluxo e digitalização exigem mais controle de versão, rastreabilidade e organização técnica. Isso inclui garantir que rótulos, bulas e FDS estejam corretos, atualizados e coerentes com o registro aprovado e com a estratégia de lançamento do produto.
6. Prepare o pós-registro com antecedência
Ajustes posteriores podem consumir tempo e reduzir velocidade comercial se não forem planejados desde o deferimento.
7. Estruture a documentação de lançamento
Antes de colocar o produto no mercado, valide a elaboração de rótulos, bulas e FDS com suporte técnico especializado. Essa etapa ajuda a reduzir inconsistências, melhora a comunicação regulatória e dá mais segurança ao processo de comercialização.
Sua empresa está preparada para transformar um registro deferido em produto efetivamente lançado no mercado?
Além do acompanhamento regulatório, essa etapa exige rótulos, bulas e FDS tecnicamente consistentes, atualizados e alinhados às exigências aplicáveis. A Sudeste apoia empresas nesse processo com serviços especializados de elaboração e revisão documental, contribuindo para mais segurança regulatória, agilidade no lançamento e melhor organização do pós-registro.
Para empresas que buscam mais eficiência nessa etapa, contar com um parceiro técnico pode reduzir retrabalho e acelerar a entrada do produto no mercado. A Sudeste oferece suporte na elaboração de rótulos, bulas e FDS, além de apoiar rotinas de gestão documental e conformidade para fabricantes, registrantes e distribuidores que precisam lançar produtos com maior segurança regulatória.
Preencha formulário abaixo e solciite já o seu orçamento:
Conclusão
O recorde de bioinsumos 2025 mostra que o setor entrou em uma fase mais dinâmica, mais competitiva e mais estratégica. Os 912 registros concedidos pelo MAPA, com destaque para 162 bioinsumos e 323 produtos técnicos, confirmam uma agenda regulatória mais ativa e alinhada à transformação do mercado. Para os fabricantes, esse cenário também amplia a importância das rotinas de pós-registro e da preparação documental necessária para que os produtos avancem com mais organização para o mercado.
Quando essa leitura é combinada com os 470 produtos formulados deferidos pelo Ibama em 2025, com predominância de suspensão concentrada, forte presença de Classe II e maior incidência de ingredientes como protioconazol e trifloxistrobina, o cenário fica ainda mais claro: há volume, há competição e há necessidade crescente de inteligência regulatória e organização documental.
Para as empresas, a mensagem é objetiva. Não basta acompanhar o número de registros. É preciso interpretar o que eles significam para portfólio, concorrência, governança documental e estratégia de crescimento. E isso inclui dar a devida atenção a documentos como rótulos, bulas e FDS, que fazem parte da estrutura necessária para transformar aprovação regulatória em operação comercial mais organizada e segura

Bruna Spinola
Gerente de assuntos regulatórios e especialista na legislação de produtos químicos. Membro das Comissões de Estudo da ABNT: CB-10 (Informações sobre segurança, saúde e meio ambiente, relacionados a produtos químicos) e CB-16 (transporte de produtos perigosos).





